Tenho estado ausente no blog pois estou com maior carga horária de estudo breve voltarei a moderar
Ausência
março 9, 2011Experimento: Água de copo de cabeça pra baixo
dezembro 1, 2010Materiais:
1- Copo
2- papel grosso ou cartão
Experimento:
1) Encha o copo até o limite, de água
2) Coloque o papel cartão na boca do copo
3) Certifique-se de que não ficou nenhuma bolha de ar lá dentro (se ficar bolhas de ar, não funciona… ou melhor, funciona… mas pra te deixar bem ensopado)
4)Pegue o copo, com uma das mãos pressionando o cartão contra o copo e o vire de ponta cabeça. Bem devagar… tire a mão do cartão. TADAM!! Ele vai ficar paradinho e água não vai cair!
Explicação:
A água se mantem no copo porque a pressão atmosférica é bem mais forte que a pressão exercida pela água contra o cartão.
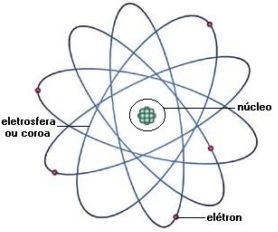
Modelo atômico de Rutherford
novembro 26, 2010A partir do século passado, vários cientistas realizaram diversos experimentos que demonstraram que o átomo é por partículas ainda menores, subatômicas.
Para verificar se os átomos eram maciços, Rutherford bombardeou uma finíssima lamina de ouro (de aproximadamente 0,0001cm) com pequenas partículas de carga positivas, denominada partículas alfa, emitidas por um material radioativo.
As observações feitas durante o experimento levaram Rutherford a tirar uma serie de conclusões.
Observaçoes:
1-Grande parte das partículas alfa atravessa a lâmina sem desviar o curso.
2-Poucas partículas alfa (1 em 20000) não atravessam a lâmina e voltavam.
3-Algumas partículas alfa sofriam desvios de trajetória ao atravessar a lâmina.
Conclusões:
1-Boa parte do átomo é vazio. No espaço vazio (eletrosfera) provavelmente estão localizados os elétrons.
2-Deve existir no átomo uma pequena região onde esta concentrada sua massa (o núcleo).
3-O núcleo do átomo deve ser positivo, o que provoca uma repulsão nas partículas alfa (positivas).
A comparação do número de partículas alfa que atravessavam a lâmina com o número de partículas alfa que voltavam levou Rutherford a concluir que o raio do átomo é 10 mil vezes maior que o raio do núcleo. A partir dessas conclusões, Rutherford propôs um novo modelo atômico, semelhante ao sistema solar.
Experimento: Amido de Milho + Água = Fluido Não Newtoniano
novembro 20, 2010Materiais:
1- Amido de Milho (maizena)
2- Água
3- Bacia ou vasilha
Experimento:
1) Encha a bacia ou a vasilha com água
2) Coloque o amido na bacia
3) Misture bem
4) Veja os resultados
Vídeo
Explicação Científica:
Substâncias fluidas que têm a sua viscosidade aumentada quando submetidas à forças externas são chamadas de fuidos não-newtonianos. No caso da mistura coloidal de amido com água, as partículas de amido “se esfregam” quando tentam se mover e daí vem a sua alta viscosidade. Mas, quando fazemos força externa sobre este colóide, o atrito de esfregação entre as partículas cresce bastante a ponto de oferecer uma resistência muito maior do que a esperada e que faz com que a mistura líquida mais pareça um sólido
Carbonizando açúcar
novembro 18, 2010Materiais necessários:
1-Um béquer de 100 mL ou outro
2-recipiente que suporte calor
3-60g de açúcar granulado
4-60 mL de ácido sulfúrico
5-concentrado
6-Um bastão de vidro
7-Luvas de borracha
8-Óculos de proteção
Agora mãos a massa
1)Antes de começar, coloque as luvas de borracha nas mãos e ponha os óculos, vá para um local arejado, ou preferencialmente dentro de uma capela com exaustão. Apenas pessoas treinadas devem tentar este experimento.
2)Coloque no béquer de 100 mL, (ou outro recipiente que suporte calor), 60g de açúcar granulado.
3)Adicione 60 mL de ácido sulfúrico concentrado dentro do béquer que contém o açúcar. Já com as luvas nas mãos, mexa o conteúdo do béquer com o bastão de vidro até ficar uma pasta marrom. Retire o bastão e observe.
segue o video:
O que acontece.
O ácido sulfúrico concentrado reage com o açúcar, formando água, carbono e muito calor, o que explica as bolhas e a fumaça produzida, além do cheiro característico de açúcar derretido.
Quando olhamos para a estrutura da sacarose, vemos que não existem moléculas de água presente, mas sim, grupos OH e átomos de hidrogênio ligados aos carbonos. São estes grupos OH, também conhecidos como hidroxilas que fazem com que o açúcar seja tão solúvel na água. Quando o ácido reage com o açúcar, ele retira os OH e os H, formando assim H2O que vai sendo evaporado pelo calor da reação.
Já o carbono é essa massa preta que cresce dentro do béquer. Por isso o açúcar é chamado de carboidrato, ele contém além de carbonos muitos hidrogênios e oxigênios, em uma proporção de 2:1 como na água.
CUIDADO!!!
O ácido sulfúrico concentrado é corrosivo e provoca queimaduras graves. Use sempre luvas de borracha para manipulá-lo. Em caso de contato com a pele lave imediatamente com muita água. Caso você derrame um pouco na bancada ou no chão, neutralize com bicarbonato de sódio e lave com água. A massa de carbono deve ser lavada antes de ser descartada no lixo comum.
FONTE: PONTO CIÊNCIA
Experimento: Água que gira não cai
novembro 18, 2010Materiais Nessesários:
1-Uma caneca
2-Um fio de barbante de aproximadamente 90 cm
3-Tampinhas de garrafa (opcional)
4-Água
Feito isso, troque as tampinhas por água e repita o procedimento. O vídeo abaixo mostra a realização do experimento. No vídeo é utilizado corante na água para facilitar a filmagem.
É importante, em ambos os procedimentos, observar que existe uma velocidade mínima para que nada caia da caneca.
Uma caneca cheia de água não poderia ser colocada de cabeça para baixo sem que seu conteúdo caísse.
No entanto, quando a caneca atinge uma velocidade mínima e passa no ponto mais alto da trajetória com essa velocidade a queda da água não é observada
Fonte: pontociencia
Foguete de Água e Ar Comprimido
novembro 7, 2010Materiais Nessesários:
– Uma garrafa pet 2 L
– Água para preencher a metade da garrafa
– Suporte
– Bomba de encher bola de futebol
– Rolha
Montagem:
1- Preencha metade da garrafa com água
2- Encaiche a rolha no pito da bomba de encher
3- Coloque a rolha com a bomba na boca da garrafa
4- Arranje algum tipo de suporte ou encosto
5- Comece a bombear e logo verá os resultados
6- A garrafa voa
Experimento: Ovo na garrafa (demonstra Pressão Atmosférica)
novembro 6, 2010Olá denovo, aqui vai mais um experimento:
Materiais nessesários:
-Um ovo cozido sem casca
-uma garrafa com gargalo largo
-fosforos
-alcool
-algodão
1- Molhe o algodão com um pouco de alcool.
2- Coloque o algodão dentro da garrafa de vidro.
ATENÇÃO: Feche a garrafa de álcool e afaste-a antes de acender o fósforo.
3- Risque três palitos de fósforo e jogue dentro da garrafa de vidro.
4- Tampe a boca da garrafa com o ovo cozido
ai vai um video
Explicação:
Os fósforos ao serem jogados dentro da garrafa entram em contato com o algodão molhado com álcool.Ocorre a combustão do álcool(C2H5OH+3O2=>3H2O+2CO2) consumindo parte do oxigênio presente na garrafa. O ar que não foi consumido se aquece e sai da garrafa, pois fica menos denso. A partir do momento que colocamos o ovo no gargalo do frasco passamos a ter um sistema fechado. Ou seja, quando o gás inicia sua contração(isso ocorre à medida que a temperatura diminui) a pressão no interior do frasco baixa para níveis inferiores. Nesse instante, o ovo vai ser forçado a entrar no frasco, pois a pressão fora da garrafa , pressão atmosférica, é maior que a pressão dentro da garrafa. Como consequência a diferença entre a pressão no exterior do frasco e no interior deste diminui.
Como Fazer Hidrogênio em Casa!
março 13, 2010Acima De Tudo CUIDADO! So faça isso com o concentimento de seus
pais esse gás é altamente inflamavel!
Você precisa de :
-2 colheres de sopa de soda caustica da mais forte
-um pouco de agua(de torneira)
-pedacinhos pequenos de papel aluminio ou pode ser pedacinhos de latinhas de refri
-garrafa pet
-bexiga de borracha ou saco plastico
Como Fazer:
1-Pegue a as colheres de soda caustica e coloque na agua
2- misture bem e coloque o papel aluminio
3-rapidamente coloque a bexiga na boca da garrafa e se afaste
4-quando a bexiga estiver cheia com cuidado chegue perto da garrafa tire-a da boca da garrafa e se afaste
5- amarre a bexiga de modo que nao saia o hidrogenio
6-Solte-a e ela irá voar 😀
7-Se quiser fazer uma bola de fogo, amarre a bexiga na ponta de uma madeira e bote um vela acesa a uma certa distancia, segure a madeira e aproxime a bola até a vela e espere estourar
Não me responsabilizo por nada que acontecer com você, abaixo um video que mostra outras coisas que se pode fazer nesse experimento
Nao faça o que esses loucos fazem
desculpem pelos erros… hehehe
Tensão Superficial
março 2, 2010Ingredientes:
1 prato fundo
um pouco de leite
corantes de alimento (pelo menos duas cores diferentes)
1 palito de dente
detergente de cozinha
Como Fazer:
1. Coloque um pouco de leite num prato fundo e deixe descansando alguns minutos para que o leite esteja sem se mover no prato.
2. Pingue algumas gotas de corantes de alimentos de cores diferentes. Em nossa experiência, colocamos uma gota de corante amarelo, um de corantes vermelho, uma de azul e uma de corante rosa. NÃO MISTURE OS CORANTES!
3. Pegue um palito de dente e molhe a pontinha com um pouco de detergente para louças. Não é necessário colocar muito detergente, só coloque um pouco na ponta do palito. Retire o excesso (se ficar como uma gota).
4. Rapidamente, coloque o palito no meio de alguma mancha de tinta. Aqui, nós fizemos assim: primeiro o palito foi colocado no meio da mancha amarela – e… PUFF!… o amarelo explodiu!
Depois, colocamos o mesmo palito na mancha azul e ela explodiu!!!
Com o mesmo palito, na mancha rosa… PUFF… de novo, explodiu!!!!
5. Você pode, agora, “passear” com o palito através das cores! Elas se misturam de uma forma divertida, formando manchas coloridas que se misturam em ondas. Fica bem legal!
Explicação:
Quando colocamos o corante na superfície do leite, eles não se misturaram – cada corante formou uma mancha separada da outra.
No momento que colocamos o palito de dente com um pouquinho de detergente dentro das manchas, elas pareciam explodir!
Isso que vimos aqui foi um exemplo de como a tensão superficial age num líquido e como ela pode ser rompida pelo detergente.
A tensão superficial acontece porque as moléculas de leite na superfície sofrem uma grande atração entre elas. No interior do líquido, todas as moléculas do leite sofrem essas mesmas forças de atração, mas em todas as direções. As moléculas de leite na superfície sofrem a atração apenas das moléculas na horizontal e das outras que estão abaixo, já que em cima tem apenas AR.
Como o número de moléculas se atraindo é menor, existe uma “compensação”: uma força maior de atração acontece na superfície, formando quase uma “pele” acima do leite. É a chamada TENSÃO SUPERFICIAL. O detergente consegue ROMPER a tensão superficial e as cores explodem! E depois se misturam formando padrões de cores incríveis quando você movimenta o palito…
Nota: se você tentar misturar os corantes movimentando um palito sem detergente, também será possível ver padrões interessantes, mas não serão tão bem misturados como da forma que fizemos aqui.
Aí vai um video mostrando outras experiencias com tensão superficial e inclusive essa do leite

![7cc9196a798a53e78d9c150ef350c3a5[2]](https://quimicomaluco.files.wordpress.com/2010/11/7cc9196a798a53e78d9c150ef350c3a52.jpg?w=300&h=225)

